Blóðþorri – ISAV – Infectious Salmon Anemia Virus
Smitefni
Infectious Salmon Anemia Virus
Veiran er af ætt Orthomyxoviridae og tilheyrir ættkvísl Isavirus. Veiran ber veiruhjúp og er 100-130nm að þvermáli.
Mikilvægt er að þekkja muninn á ISAV-HPR0 og ISAV-HPRdel veiruafbrigðunum. Það er einungis það síðarnefnda sem veldur blóðþorra en það fyrrnefnda sýkir aðens tálknin og veldur ekki sjúkdómseinkennum. ISAV-HPR0 getur þó stökkbreyst og orðið að hættulega ISAV-HPRdel afbrigðinu og því er það öruggast að halda þessu meinlausa veiruafbrigði frá eldinu.
Móttækilegir hýslar
Í náttúrunni hefur ISA veiran einungis valdið sjúkdómi í Atlantshafslaxi (Salmo salar) í eldi svo vitað sé. Veiran hefur þó verið greind í regnbogasilungi (Oncorhynchus mykiss) í Írlandi og coho laxi (Oncorhynchus kisutch)í Chile. ISA veiran hefur verið greind með RT-PCR í villtum atlantshafslaxi, urriða og sjóbirting en einungis var um einkennalausa smitbera að ræða.
ISA veiran hefur fundist í allnokkrum fiskitegundum í kjölfar smits í tilraunaskyni. Hér má nefna urriða og sjóbirting (Salmo trutta), regnbogasilung (Oncorhynchus mykiss), bleikju (Salvelinus aplinus), síld (Clupea harengus) og atlantshafsþorsk (Gadus morhua).
Veiran er hættulaus mönnum og öðrum spendýrum.
Smitleiðir
Megin smitleiðin er að öllum líkindum yfir tálknin, en smit í gegnum meltingarveg er ekki útilokað. Helstu markfrumur ISA veirunnar eru æðaþelsfrumur fisksins, sem þekja innra byrði æðanna. Framleiðsla nýrra veira getur farið fram í öllum líffærum líkamans, en mest er framleiðslan í hjarta. Veiran smitast áfram með vessum smitaðs fisks.
Langstærstur hluti blóðþorratilfella á heimsvísu eru greind í laxi í sjókvíaeldi en nokkur tilfelli hafa komið upp í seiðaeldishluta framleiðslunnar, þar á meðal eitt tilfelli hjá kviðpokaseiðum. Á Íslandi hefur blóðþorri aðeins greinst í sjókvíaeldi á Austfjörðum hingað til.
Það getur tekið mánuði fyrir smit að berast á milli kvía, en ef veiran fær að fjölga sér óáreitt getur hún breiðst til allra kvía kvíabólsins og jafnvel til annarra nærliggjandi kvíabóla. Flutningur á sýktum lifandi fiski er einnig mikilvæg smitleið og getur borið smit yfir langar vegalendir. Blóðvatn frá sláturhúsum getur einnig verið smitandi sé verið að slátra ISAV smituðum fiski, ef sótthreinsun frárennslis er ekki sem skyldi. Smitist seiði á leið frá seiðastöð til kvíabóls geta komið upp smit í mörgum kvíum samtímis. Gæta þarf varúðar þegar bátar og/eða fólk ferðast á milli eldisstöðva til að varna því að smit berist á milli.
Sjúkdómseinkenni
Veiran ræðst eins og fyrr segir á æðaþelsfrumur fisksins sem þekja innra byrði æðanna og veldur blæðingum í öllum helstu líffærum og blóðleysi (anemia) í framhaldinu.
Helstu ytri sjúkdómseinkenni blóðþorra eru mjög föl tálkn, útstandandi augu, bjúgmyndun í hreistursslíðri og blæðingar á kvið. Innri sjúkdómseinkenni geta verið blóðfyllt innri líffæri, þá sérstaklega lifur, milta og nýra, vökvi í kviðarholi sem og blæðingar í lífhimnu og vöðva.
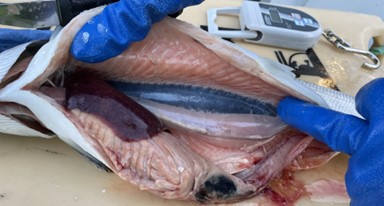

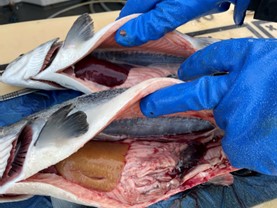
Hegðunarleg einkenni eru einna helst slappleiki þar sem fiskurinn heldur sig upp við nótina og sýnir skert viðbragð við hreyfingu ofan vatnsyfirborðs.
Afföll geta verið mjög breytileg frá einni kví til annarar. Dagleg afföll í sýktri kví geta verið á bilinu 0,5-1‰ í langan tíma en heildarafföll geta endað í yfir 90%.
Greining
Ef grunur leikur á að blóðþorri sé til staðar í laxi skulu viðeigandi sýni tekin og send til greiningar. Það eru yfirleitt klínísk einkenni og affallasaga sem fyrst vekja grun um sjúkdóminn. Vefjafræðisýni af öllum helstu líffærum eru sett í formalín og PCR sýni úr hjarta sett í viðeigandi PCR glös. Ef um blóðþorra er að ræða koma í ljós vefjafræðibreytingar sem gætu verið vegna ISA veirunnar og PCR niðurstöður sem sýna fram á að ISA veiran sé til staðar í vefjum fisksins staðfesta svo greininguna.
Þolmörk veirunnar utan hýsilsins
Erfitt er að segja til um hversu lengi veiran lifir utan við hýsilinn vegna margra þátta í umhverfinu sem geta bundið eða haft áhrif á meinvirkni veirunnar. Gerðar hafa verið rannsóknir á ISA veirum sem ræktaðar hafa verið á rannsóknastofum þar sem fram kom að meinvirkni (virulence) veirunnar breyttist ekki við 15°C í 10 daga eða 4°C í 14 daga.
Afleiðingar smits
Blóðþorri (ISAV) er tilkynningaskyldur dýrasjúkdómur. Slátra þarf öllum fiski í stöðvum þar sem ISAV-HPRdel greinist vegna hættu á smiti, nærliggjandi kvíar eru undir stöðugu eftirliti.
Óvirkjun veirunnar eða minnkun á meinvirkni
UV geislun:
ISA þolir illa UV geislun. Í dauðhreinsuðu ferskvatni minnkaði meinvirkni veirunnar um 3-log (99,9%) þegar notast var við UV geislun með styrk 35 J/m2. Í dauðhreinsuðu sjóvatni náðist sama minnkun meinvirkni við 50 J/m2. Til að ná sömu minnkun meinvirkni í úrgangsvatni frá fiskasláturhúsi þurfti að notast við 72 J/m2 geislunarstyrk.
Ósón:
Ósónmeðhöndlaður sjór (4 mínútur með 8 mg/ml, 600-750mV oxunar-afoxunarspenna (redox potential)) gæti óvirkjað veiruna að fullu.
Sótthreinsiefni:
– Veiran þolir ekki
- 100 mg/ml af klór í 15 mínútur
- Virkon-S (1%) í 20 mínútur
- Buffodine (108 ppm) í 15 mínútur
- Joðófór (100-200 mg/l) í 5 mínútur
- Halamid (Kloramin-T) (2%) í 10 mínútur
- Sodium hydroxýð (pH>12) í 7 klst
- Formaldehýð (0,5%) í 16 klst
Sýrustig: Sýrustig (pH gildi) 4 eða 12 í 24 tíma óvirkjaði meinvirkni ISA veirunnar í vef úr ISA sýktum fiski.
Hitastig: ISA veira sem ræktuð hefur verið í frumurækt lifir vikum saman við lágt hitastig en 56°C í 30 mínútur óvirkar meinvirkni veirunnar að fullu.
Heimildir
Manual of Diagnostic Tests for Aquatic Animals 2009, Kafli 2.3.5 Infectious Salmon Anaemia.
Matvælastofnun. www.Mast.is
Correlation of Virus Replication in Tissues with Histologic lesions in Atlantic salmon experimentally infected with Infectious Salmon Anemia virus. E.Moneke et al. 2005